近日,权威期刊Proceedings of National Academy of Sciences在线发表了我校生命科学与技术学院王琛教授团队的最新科研成果——“STING inhibitors target the cyclic dinucleotide binding pocket”。课题组成员博士后洪泽,硕士研究生梅家豪和博士后李晨辉为文章的共同第一作者,王琛教授和哈佛大学医学院Judy Lieberman教授为本文的共同通讯作者。
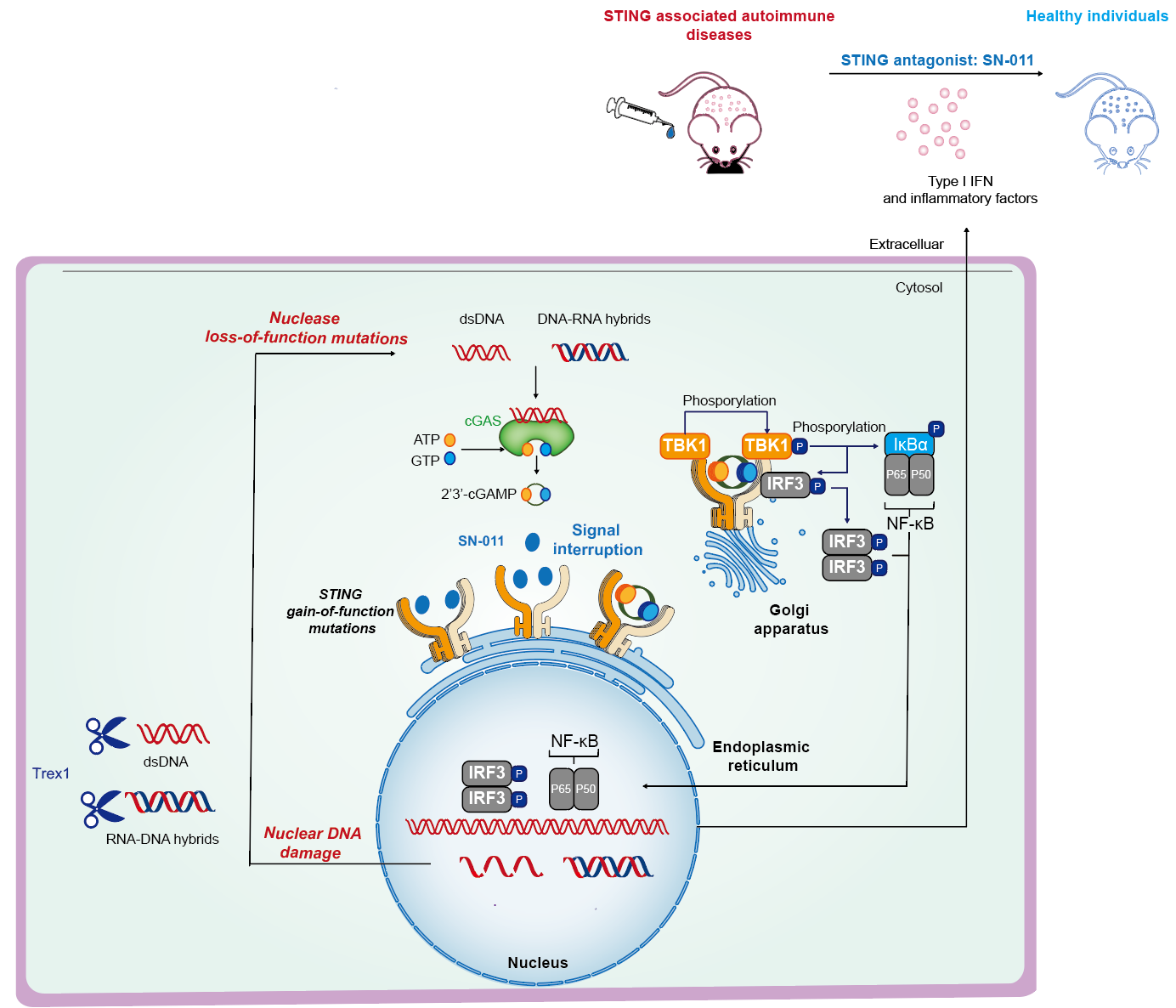
固有免疫系统是机体抵抗病原微生物入侵的第一道防线,能激活机体的适应性免疫共同清除入侵的病原体,维持机体的稳态。 胞浆DNA 介导的 cGAS-STING 固有免疫信号通路的激活在机体抵抗 DNA 病毒和逆转录病毒等多种病原体中发挥着重要的作用。然而越来越多的研究发现,STING 信号通路的异常激活促进无菌性炎症疾病包括自身免疫疾病、神经退行性疾病、代谢紊乱疾病和癌症的发生和发展。因此开发靶向 STING 蛋白的小分子抑制剂或激动剂,具有重要的基础研究意义和潜在的临床应用价值 。
该团队通过靶向STING蛋白的化合物筛选和生物活性评价发现小分子SN-011,及其同一骨架的小分子衍生物均具有强效的靶向STING信号通路的抑制作用。机制研究进一步证实小分子SN-011能特异性结合在STING蛋白与其内源性配体分子2’3’-cGAMP结合的口袋内。

婴儿期发生的 STING 相关的血管样病变 (STING-associated vasculopathy with onset in infancy, SAVI)是由于编码 STING 蛋白的基因 TMEM173突变导致STING蛋白异常激活引起的罕见自身免疫疾病。在过表达STING相关的突变体的细胞内,SN-011能显著抑制下游过度激活的免疫和炎症细胞因子。在Aicardi-Goutières syndrome 的小鼠疾病模型(Trex1-/-)中,SN-011能显著改善小鼠多组织器官的免疫损伤,且延长疾病小鼠的生存时间。此外,越来越多的研究发现STING蛋白的异常激活与神经退行性疾病,代谢紊乱疾病和心脑血管疾病的进展密切相关。因此,该团队发现的STING小分子抑制剂SN-011不仅可以作为先导化合物进行优化,更具有广泛的应用前景。
该研究工作获得国家自然科学基金重点项目、面上项目、国家重点研发计划、中国药科大学双一流学科创新团队、江苏省双创团队和天然药物活性组分与药效国家重点实验室研究课题等资助。中国药科大学药物科学研究院孙宏斌教授,余文颖教授和中科院巴斯德所刘星教授亦对本研究做出了重要的贡献。
(供稿单位:生命科学与技术学院,撰写人:洪泽)

